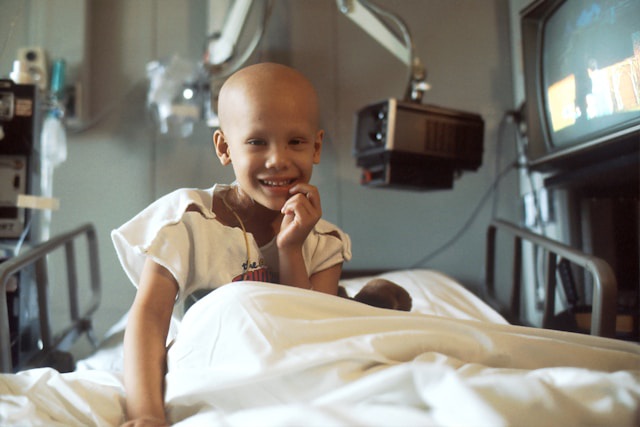
Explorer les différentes approches thérapeutiques pour traiter la leucémie
La leucémie demeure l’un des cancers les plus complexes à traiter en raison de la diversité de ses formes et de ses manifestations cliniques. En 2026, la prise en charge de cette maladie s’appuie sur un arsenal thérapeutique évolutif, combinant des techniques traditionnelles avec des innovations de pointe. La compréhension approfondie des spécificités biologiques de chaque type de leucémie permet désormais de proposer une stratégie personnalisée, modulée selon le profil du patient, son âge, ses antécédents médicaux et les caractéristiques moléculaires de sa maladie. Cette approche multidisciplinaire offre un nouvel espoir aux malades, tout en posant des défis importants liés à la gestion des effets secondaires et à la préservation de la qualité de vie. L’exploration des différentes options disponibles chimiothérapie, radiothérapie, immunothérapie, greffe de moelle osseuse ou thérapies ciblées révèle à la fois la complexité du parcours thérapeutique et la richesse des avancées scientifiques récentes dans le domaine des soins oncologiques.
Les fondements de la chimiothérapie dans le traitement de la leucémie : pratiques et défis
La chimiothérapie demeure la pierre angulaire du traitement de la leucémie, notamment pour les formes aiguës comme la leucémie myéloïde aiguë (LMA) et la leucémie lymphoïde aiguë (LLA). Fondée sur l’administration de médicaments cytotoxiques, cette thérapie vise à détruire les cellules leucémiques en interférant avec leur capacité à se multiplier. En 2026, les protocoles ont gagné en sophistication, combinant souvent plusieurs agents pour maximiser les chances de rémission. La chimiothérapie d’induction constitue la première phase cruciale, dont l’objectif est d’éliminer massivement les cellules cancéreuses présentes dans la moelle osseuse et le sang. Cependant, cette phase intensive ne convient pas à tous les patients, notamment aux personnes âgées ou fragilisées, qui risquent des complications sévères.
Pour ces patients, des alternatives comme l’azacitidine ou le venetoclax offrent une option plus douce pour soigner une leucemie avec efficacité. Ces molécules ralentissent la progression de la maladie tout en réduisant les effets secondaires associés aux traitements classiques. Une fois la phase d’induction réussie, le traitement post-rémission, dit consolidation, vise à éradiquer les cellules leucémiques résiduelles. Il permet de diminuer sensiblement le risque de rechute. La chimiothérapie de consolidation peut s’accompagner d’une greffe de cellules souches hématopoïétiques pour restaurer une production normale des cellules sanguines.
Au-delà de leur efficacité, les traitements chimiothérapeutiques comportent une charge non négligeable d’effets indésirables. Nausées, vomissements, perte d’appétit, fatigue intense, infections dues à la neutropénie ou encore perte temporaire des cheveux sont autant d’épreuves que doivent surmonter les patients. Ces manifestations impactent profondément la qualité de vie, nécessitant une gestion médicale rigoureuse et un accompagnement personnalisé. Par ailleurs, certaines toxicités à long terme, telles que les troubles cardiaques ou les déficits immunitaires persistants, restent des défis importants dans le suivi de ces patients.
L’adaptation des doses et la surveillance attentive permettent toutefois de limiter ces risques. Aujourd’hui, les équipes médicales s’appuient également sur des outils technologiques et biologiques avancés pour ajuster le traitement en fonction de la réponse individuelle. Par exemple, le dosage précis des biomarqueurs sanguins aide à anticiper la rémission ou la rechute, offrant ainsi une meilleure maîtrise du calendrier thérapeutique. Bien que la chimiothérapie soit parfois perçue comme lourde, elle reste un pilier incontournable des approches thérapeutiques, particulièrement efficace pour induire un premier contrôle rapide de la leucémie.
La greffe de moelle osseuse : un traitement complexe mais salvateur
La greffe de moelle osseuse, ou greffe de cellules souches hématopoïétiques, constitue une étape majeure dans la prise en charge de nombreuses leucémies, notamment lorsque la maladie est réfractaire ou en phase de rechute. Cette intervention consiste à remplacer la moelle osseuse du patient par des cellules saines provenant d’un donneur compatible. Cette procédure vise à restaurer la capacité de la moelle à produire des cellules sanguines normales tout en bénéficiant d’un effet immunologique appelé « effet greffon », où les cellules du donneur détruisent les cellules leucémiques restant dans l’organisme.
En 2026, les techniques de greffe se sont considérablement améliorées, réduisant les risques liés à la réaction du greffon contre l’hôte (GVH), un phénomène redouté qui peut compromettre gravement la réussite de l’opération. Les nouvelles méthodes de typage HLA (antigènes leucocytaires humains) et l’utilisation de protocoles immunosuppresseurs spécifiques ont contribué à mieux contrôler ces complications. Néanmoins, la greffe demeure un traitement lourd, réservé en général aux patients pouvant supporter la procédure sur le plan général et immunitaire.
Par exemple, un patient jeune atteint d’une leucémie myéloïde chronique (LMC) réfractaire aux traitements ciblés peut être un candidat idéal pour la greffe. Pour lui, cet acte représente une possibilité de guérison durable. Cependant, le processus est long et complexe, incluant une phase de conditionnement où la moelle osseuse est préalablement détruite par chimiothérapie et/ou radiothérapie afin de faire place aux nouvelles cellules. Après la greffe, le suivi est intensif, surveillant les signes d’infections, de rejet et d’autres complications immunologiques.
Les effets secondaires liés à la greffe incluent la neutropénie sévère, une thrombocytopénie provoquant un risque hémorragique élevé, ainsi que des atteintes cutanées ou digestives. L’impact psychologique de cette procédure est également important et nécessite un soutien constant. Malgré ces contraintes, de nombreux patients témoignent d’une amélioration significative de leur état de santé après une greffe réussie, montrant la puissance thérapeutique de cette option. La greffe de moelle osseuse reste un symbole d’espoir et un levier majeur des soins oncologiques modernes dans la lutte contre la leucémie.
Les avancées de l’immunothérapie et du ciblage moléculaire dans la lutte contre la leucémie
L’immunothérapie a transformé la manière de penser le traitement des cancers, et la leucémie ne fait pas exception. Cette approche consiste à stimuler le système immunitaire du patient pour qu’il puisse identifier et détruire les cellules leucémiques. Parmi les innovations majeures, les thérapies par cellules CAR-T, qui modifient génétiquement les lymphocytes T du patient pour les rendre capables d’attaquer spécifiquement les cellules cancéreuses, ont obtenu des résultats spectaculaires dans certains cas de leucémie lymphoïde chronique ou aiguë.
Outre la thérapie CAR-T, les anticorps monoclonaux et les interférons apportent également des solutions ciblées, offrant souvent une meilleure tolérance que la chimiothérapie classique. Ces traitements peuvent être utilisés dans les situations où les patients présentent une résistance aux médicaments traditionnels ou ne sont pas éligibles à la greffe de moelle osseuse. Le ciblage moléculaire, quant à lui, repose sur l’identification de mutations spécifiques au sein des cellules leucémiques, permettant de prescrire des inhibiteurs agissant sur ces anomalies précises. Par exemple, l’utilisation d’inhibiteurs de tyrosine kinase dans la leucémie myéloïde chronique a largement révolutionné le pronostic de cette maladie.
Chacune de ces approches ouvre la voie à une médecine plus personnalisée où le traitement est adapté en fonction du profil génétique du patient et des caractéristiques moléculaires de sa leucémie. Cette précision réduit les effets secondaires systémiques tout en renforçant l’efficacité du traitement. Toutefois, ces techniques restent coûteuses et leur accès peut être limité dans certains centres. Leur intégration dans la pratique courante nécessite également un suivi rigoureux pour évaluer les réponses et gérer les effets immunitaires parfois lourds, notamment dans le cas des cellules CAR-T.
À titre d’exemple, plusieurs études récentes montrent que les patients traités par immunothérapie ciblée peuvent atteindre une rémission prolongée, même en cas de rechute après une chimiothérapie classique. Cette nouvelle frontière thérapeutique promet une meilleure maîtrise du cancer et renouvelle les espoirs face à la leucémie. Néanmoins, cette avancée s’accompagne aussi de défis, comme la gestion des effets indésirables à long terme et la nécessité d’une coordination étroite entre hématologues, immunologues et oncologues.